分子数相同的一氧化碳和二氧化碳,它们的质量比为
A.1:2
B.2:1
C.7:11
D.11:7
对258人提供帮助
分析:利用不同物质的质量与物质的相对分子质量之比等于物质中所含分子个数比来进行计算.
解答:设一氧化碳的质量为m,二氧化碳的质量为n
则有: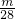 :
: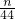 =1:1
=1:1
解之得:m:n=7:11
故选C
点评:本题主要考查学生根据化学式进行有关计算的能力,要理解此题可以联想:2CO+02 2CO2,化学方程式所表示的意义,第一表示参加反应和生成物的分子个数之比为一氧化碳和二氧化碳的分子数之比为1:1,第二还表示二者参加反应和生成的质量比为28:44.
2CO2,化学方程式所表示的意义,第一表示参加反应和生成物的分子个数之比为一氧化碳和二氧化碳的分子数之比为1:1,第二还表示二者参加反应和生成的质量比为28:44.