有5.8g铁的氧化物,加热时用氢气充分还原可生成1.8g 水,此铁的氧化物化学式为
A.FeO
B.Fe2O3
C.Fe3O4
D.无法判断
对258人提供帮助
分析:根据水中氧元素的质量就是铁的氧化物中的氧元素的质量,然后根据氧化物的质量求出铁元素的质量,然后算出化合物中两种元素的原子个数比即可.
解答:1.8g 水中氧元素的质量=1.8g×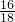 ×100%=1.6g,则5.8g铁的氧化物中铁元素的质量=5.8g-1.6g=4.2g;
×100%=1.6g,则5.8g铁的氧化物中铁元素的质量=5.8g-1.6g=4.2g;
则氧化物中铁、氧两种元素的原子个数比=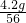 :
: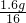 =3:4
=3:4
故选C
点评:此题计算原子个数比是最简单的计算方法,如果用质量分数来计算的话,需要依次计算各个选项中的氧元素的质量分数,耗时较多,不利于节约时间.