【题文】向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤,下列说法正确的是

资料:A的溶解度
温度/℃
20
30
40
50
60
溶解度/g
37.2
41.4
45.8
50.4
55.2
A.②中A的质量分数最大 B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液 D.①③④⑤中没有固体存在
对258人提供帮助
A、根据A物质在30℃的溶解度为41.4g、60℃的溶解度为55.2g,可判断41.4g物质A在25℃时不能完全溶解而在60℃时可以全部溶解且为不饱和溶液,则溶液②的溶质质量分数小于溶液③的溶质质量分数.故A不正确;
B、溶液③为60℃时100g水溶解41.1gA物质所形成的溶液,溶液中溶质的质量分数=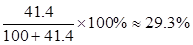 溶液⑤为50℃时100g水溶解50.4gA的饱和溶液,溶液中溶质的质量分数=
溶液⑤为50℃时100g水溶解50.4gA的饱和溶液,溶液中溶质的质量分数=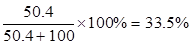 ,故B不正确;
,故B不正确;
C、综合A、B项分析可知:溶液②⑤为饱和溶液;60℃A的溶解度为55.2g,溶液④为60℃时100g水溶解50.4gA,可判断此时溶液为不饱和溶液;故C不正确;
D、根据20℃A的溶解度为37.2g可判断,25℃时37.2gA溶解在100g水中形成不饱和溶液,没有固体存在;综合A、B、C项分析,溶液③④均为不饱和溶液,没有固体存在;而溶液⑤恰好饱和,没有固体存在.故D正确;